超级计算机揭示了细胞膜如何阻止致癌蛋白的关闭
来自凯斯西储大学医学院的两位生物物理学家使用超级计算机来展示细胞膜如何控制一种主要致癌蛋白的形状,从而控制其功能。这种蛋白质是一种叫做K-Ras的小酶,附着在细胞膜上,在那里它可以感知来自细胞外的信号。在癌症期间,功能失调的K-Ras然后激活细胞内可导致肿瘤生长和转移的蛋白质。K-Ras是一种麻烦的分子开关,在许多癌症,特别是胰腺癌中永远“开启”。该研究不仅提供了一种研究K-Ras的新方法,该方法仅为1/100000英寸,而且还显示了蛋白质的几何结构如何解释其在癌症进展中的作用。
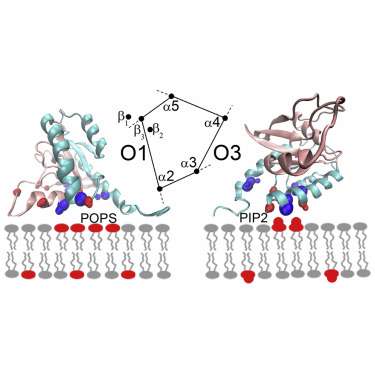
在期刊结构中描述的一系列模拟中,研究人员发现了细胞膜中的脂肪和电荷如何完全改变K-Ras的方向。膜中一种特定类型的脂肪或脂质中的太多会移动并转变K-Ras,将其活性部分推离膜并进入细胞,在那里它可以传递致癌信号。其他膜脂有助于将癌症驱动蛋白的一部分折叠起来,使其与膜紧密接触,从而使其失活。
“实验研究表明,致癌的K-Ras蛋白在膜上的定位对其功能起重要作用,”凯斯西储大学医学院生理学和生物物理学研究负责人,Matthias Buck博士说。案例综合癌症中心的成员。“我们发现一种特殊类型的膜脂质PIP2将蛋白质转变为能够使其活跃并促进癌症的方向。”
该发现表明,细胞膜中PIP2的有限浓度可以帮助保持有害的K-Ras蛋白被膜隐藏在“关闭”位置。“某些细胞信号传导脂质改变致癌Ras蛋白的活性的发现,表明我们也许能够通过抑制,这使得特定小区中的信令脂质的酶与肿瘤进展干扰细胞,”巴克说。
这项研究的灵感来自巴克的合着者,哲学博士(Andrew),博士,凯斯西储大学医学院生理学和生物物理学系的博士后学者。正如巴克所说:“他仔细研究了K-Ras蛋白质的结构以及它与膜的相互作用。他发现蛋白质不是'圆球',而是'金字塔状结构'。”因此,只有五个表面可用于与膜相互作用。“
有了这一启示,研究人员在计算机模拟中研究了所有五种K-Ras方向,将蛋白质置于不同的膜上,模仿生理情况。每次模拟都允许研究人员向原子预测K-Ras如何根据膜的成分以及每个表面上的电荷范围进行自旋和定向。
“我们在计算机的'虚拟空间'中代表了我们蛋白质的所有原子。在几十年的工作中,原子如何相互作用并相互施加力,使我们能够预测蛋白质区域及其结构的运动, “巴克解释道。“通过这种方式,现代超级计算机可以模拟数百万小时的原子运动,让我们在微秒时间尺度上检查蛋白质和细胞膜行为。”
这种实时模拟需要巨大的计算机能力。“过去几年,我们很幸运能够在匹兹堡超级计算机中心获得专业的分子动力学模拟计算机,称为安东。案例高性能计算集群和俄亥俄州超级计算机中心也帮助我们实现了模拟,通常需要数周,如果不是几个月的计算机时间,“巴克说。
K-Ras长期以来一直是药物设计的首要目标。但新的研究表明,蛋白质的有害物理特性可能是由于其膜环境造成的。这种见解有助于推动癌症预防方面的新创新。Li总结道,“K-Ras-膜相互作用的特征可能引导我们进入药物设计的不同方向。而不是直接靶向K-Ras,也可以考虑膜。”
推荐内容
-
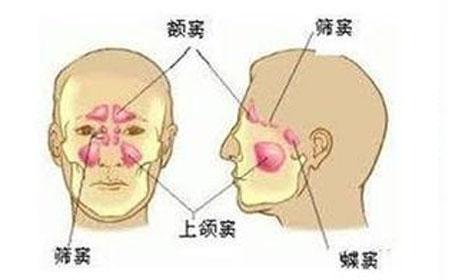
老年患者的独特慢性鼻窦炎形式
一项新的研究表明,患有慢性鼻窦炎的老年患者 - 鼻腔和鼻窦疾病经常持续多年 - 具有独特的炎症特征,可能使他们对类固醇治疗的反应性降
-
新的研究显示鱼的大脑尺寸受到栖息地的影响
繁忙的街区,越大的体验能够了解大脑,至少对南瓜籽翻车鱼,根据一项开创性研究圭尔夫大学的生物学家。太阳鱼生活在更复杂的海岸线栖息地的大
-
唐朝时人们过中秋节也会有假期吗?唐朝建立于什么时候?
蚂蚁庄园是支付宝里面的一款养成小游戏,玩家主要的目的就是让自己的小鸡快快长大。而对于小鸡长大的方式就是喂饲料。那么,对于今日蚂蚁庄
-
爸爸的关键遗传确保了健康的胚胎
生命的一个重要特征是胚胎在受精时从母亲和父亲那里得到什么。奇怪的是,中心粒,即负责细胞分裂和鞭毛运动的结构,由父亲的配子给出。...
-
【聚焦】瞒报行程致疫情在北京扩散,这个工头儿鞠躬致歉
【聚焦】瞒报行程致疫情在北京扩散,这个工头儿鞠躬致歉 原标题:【聚焦】瞒报行程致疫情在北京扩散,这个
-
美国大选实时票数更新 美媒:费城计票速度放缓
众所周知,根据美国选举制度,美国总统由选举人团选举产生,并非由选民直接选举产生,获得半数以上选举人票者当选总统。当前正在火热进...
-
科学家在临床前研究中逆转纤维化
在细胞和小鼠模型中,梅奥诊所的研究人员和合作者已经确定了一种减缓和逆转不受控制的内部瘢痕形成过程的方法,这种过程称为纤维化。这...
-
一场淡水咸水拔河比赛正在大沼泽地消失
他在木栈道霸干草okee忽略的是短暂的,蜿蜒的小路进入沼泽地国家公园梦幻世界。在木板条之外,一片宽阔的轻轻挥动的锯草延伸到地平线,在那
-
不受抗菌药和抗生素影响的细菌 通常被称为超级细菌
根据澳大利亚和英国科学家的最新研究,细菌用来抵抗旨在杀死它们的化学物质的分子机器也可以帮助生产新一代尼龙和其他聚合物的前体。对...
-
经历过“夫妻生活”的女性,这些方面瞒不住,或许还会招来羡慕
经历过“夫妻生活”的女性,这些方面瞒不住,或许还会招来羡慕 原标题:经历过“夫妻生活”的女性,这些方