肿瘤基因融合测试获得突破性进展
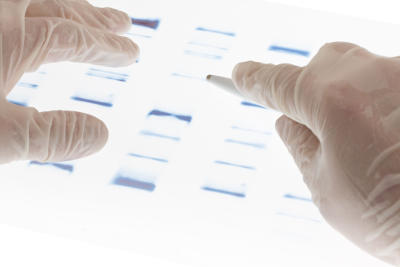
Caris Life Sciences获得了FDA突破性的设备命名,用于伴随诊断测试,旨在检测实体瘤中的成纤维细胞生长因子受体生物标志物,包括基因融合体。
MI Transcriptome CDx检测旨在帮助鉴定具有特定遗传特征和分子改变且可能对靶向疗法有反应的患者。体外诊断测试是第一个能够在所有实体肿瘤检测的基因融合,该公司表示。
总部位于得克萨斯州欧文的Caris表示,计划在今年晚些时候将该测试提交FDA上市前批准。

基因融合是被认为可以驱动肿瘤生长的遗传改变。Caris测试可以区分融合类型,并将融合与其他重排区分开。
下一代测序正在帮助肿瘤学家了解驱动癌症进展的基因变化。临床实验室已迅速采用癌症测试方法,因为它具有加速个性化疗法发展以改善患者预后的潜力。根据《分子诊断学杂志》上发表的试验实践指南概述,它被用于分子肿瘤学应用,从对整个肿瘤基因组进行临床研究测序到靶向的临床诊断基因组。
该公司表示,Caris检测是一种基于测序的下一代检测,该检测使用从福尔马林固定的石蜡包埋的组织标本中分离的RNA来检测所有类型的结构重排,包括融合,缺失,倒位和重复。
RNA测序作为一种廉价的癌症基因表达谱分析技术正变得越来越普遍。卡里斯说,它的测试能够测量基因表达,通过该过程,基因在细胞内被打开,以制造RNA和蛋白质,从而对肿瘤进行分类。该测试还可以量化导致癌症发展的剪接变体。
上个月,FDA批准了强生(Johnson&Johnson)的Balversa批准用于治疗其肿瘤中FGFR基因发生改变的转移性或局部晚期膀胱癌患者的第一种FGFR抑制剂。
用于NGS测试的CMS报销政策正在不断变化。在医疗保健组织的压力下,该机构上个月重新开放了其全国范围的确定性决定,该机构最初的决定将拒绝对患有早期癌症的Medicare受益人进行检查。基因测序平台的领导者Illumina和Thermo Fisher Scientific以及测试提供商Myriad Genetics都在努力扩大覆盖范围。
推荐内容
-
关于果蝇如何驾驭世界的新线索出现了
坐落在果蝇大脑的深处,专门的神经细胞将自己编织成一个小指南针。来自Janelia Research Campus的神经科学家的新结果阐明了该电路的结构
-
保护基因组研究中的机密性
全基因组关联研究寻找特定遗传变异与疾病发病率之间的联系,是许多现代生物医学研究的基础。但基因组信息数据库会带来隐私风险。从人们...
-
比目鱼基因提供了对性染色体进化的洞察力
半光滑舌苔(Cynoglossus semilaevis)是一种沿中国沿海养殖的海洋比目鱼,其性别主要取决于性染色体的遗传,但也受环境因素的影响。在高温
-
最古老的非洲人类基因组测序
来自非洲和近东的现代人似乎比以前想象的更早,更复杂地进行了交互,对非洲最古老的人类核DNA进行了一项研究。1这项新研究结果来自对摩洛哥
-
古代的博泰马匹未能通过现代驯化马的亲子鉴定
很长一段时间,人们认为普氏原羚的马是一种珍稀濒危物种,是世界上最后剩下的野马。许多研究人员还认为,已知最古老的驯养马匹的博泰马...
-
哈圈迷惑行为最近怎么了?哈圈热搜莫名的唱着莫名的歌事件完整版
哈圈今天怎么了,这么多人在榜上[吃瓜]只知道前因是贝贝发了一首歌?那奇沃夫评论他是活着的传奇,然后幼稚园杀手又刚好发了专辑叫《活着的
-
对细胞膜的新见解可以改善药物测试和设计
阿肯色大学对膜蛋白的研究可以促进药物的更好开发和测试。化学研究人员研究了一种从细胞中排出药物的膜蛋白,有助于抗药性。他们发现细...
-
失去基因和生存 当生命的进化越少越好
哲学家和皇帝马库斯·奥里利乌斯(Marcus Aurelius)引用了一篇科学文章,分析了基因丧失现象及其对生物进化的影响,他说:损失只不过是变化
-
科学家们指出优秀的赛马“速度基因”是如何工作的
科学家已经精确地定位的遗传基础,解释了为什么一些优秀的赛马比赛能更好地冲刺距离和其他人在更远的距离。爱尔兰科学家,从都柏林三一学...
-
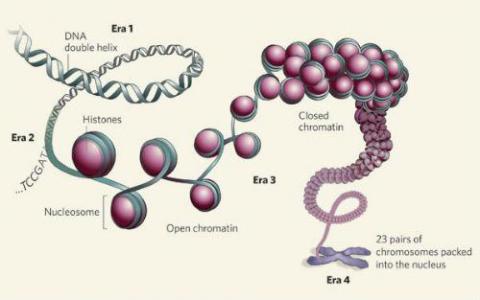
了解染色质的癌症连接
当科学家在2003年完成对人类基因组的解码时,他们认为这些发现将有助于我们更好地了解疾病,发现与癌症相关的基因突变,并导致智能医学的设