逐步重建生命逐个细胞
经过13次快速分裂后,受精的蝇卵由约6,000个细胞组成。它们在显微镜下看起来都很相似。然而,黑腹果蝇的每个细胞胚胎已经知道它是否注定要成为神经元或肌肉细胞 - 或肠道,头部或尾巴的一部分。现在,Helmholtz协会(MDC)MaxDelbrück分子医学中心柏林医学系统生物学研究所(BIMSB)的Nikolaus Rajewsky和Robert Zinzen团队分析了数千个单细胞的独特基因表达谱并重新组装胚胎从这些数据中使用新的空间映射算法。结果是虚拟飞胚在这个时间点准确显示哪些基因是活跃的。“它基本上是早期发育的转录组蓝图,”神经组织分化实验室系统生物学主管Robert Zinzen说。他们的论文作为科学在线问题的第一版发布。
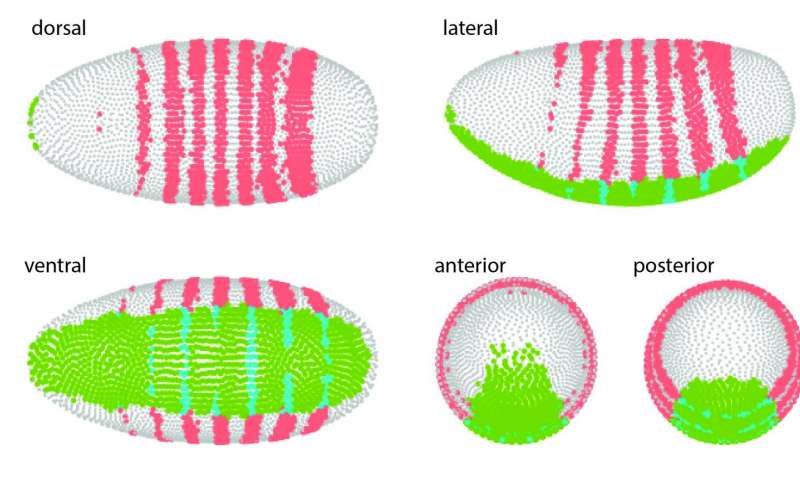
“最近才有可能大规模分析单个细胞的全基因组基因表达.Nikolaus很早就认识到这种技术的潜力,并在他的实验室中建立了它,”Zinzen说。“他开始怀疑 - 给定一个复杂的有组织组织 - 一个人能够单独从单细胞转录组数据计算全基因组空间基因表达模式。”BIMSB结合了具有不同背景和专业知识的实验室,强调了为生物问题带来计算能力的需求。事实证明,研究所不仅有完美的模型系统 -果蝇胚胎 - 来解决Rajewsky的问题,而且还有正确的人才,具有正确的专业知识,
“虚拟胚胎不仅仅是一种细胞标测运动,”基因调控元素实验室系统生物学主任Nikolaus Rajewsky说道,他在研究果蝇胚胎期间的基因调控元件15年后享受回归飞行发展的乐趣。洛克菲勒大学的博士时间。使用交互式DrosophilaVirtual Expression eXplorer(DVEX)数据库,研究人员现在可以查看大约8,000个表达基因中的任何一个在每个细胞中询问,“基因X,你在哪里表达,在什么水平?在同一时间和同一细胞中有哪些其他基因活跃?”它也适用于神秘的长非编码RNA。“不是耗时的成像实验,科学家们可以通过虚拟实验来识别新的监管机构,甚至可以获得生物机制的想法,”Rajewsky说。“通常需要数年才能使用标准方法,现在可以在几个小时内完成。”
打破第一个细胞分裂的同步性
在他们的论文中,MDC的研究人员描述了十几种新的转录因子和更多以前从未研究过的长非编码RNA。此外,他们提出了一个困扰科学家35年的问题的答案:胚胎如何破坏细胞分裂的同步性以发展更复杂的结构?
在称为原肠胚形成的过程中,形成不同的胚层,并且细胞在它们可能分化成哪些组织和器官方面受到限制。“我们相信河马信号通路至少部分地负责建立原肠胚,”Rajewsky说。该途径控制器官大小,细胞周期和细胞增殖,但从未涉及早期胚胎的发育。“我们不仅表明Hippo在苍蝇中是活跃的,而且我们甚至可以预测胚胎的哪个区域会导致有丝分裂的不同发作,从而打破同步性。这只是我们的工具有用的一个例子。了解逃避传统科学的机制。“
项目经历了艰难的酝酿期
当研究人员开始创建虚拟胚胎时,他们不知道是否可能。Drop-Seq技术是Dropf Seq技术的最重要成果,它是一种基于液滴的微流体方法,可以低成本对数千个细胞进行转录分析。这项技术是夏季学生Jonathan Alles在Rajewsky实验室新设立的。
然而,需要在原肠胚形成开始时精确选择苍蝇胚胎。罗伯特·辛森实验室的博士生菲利普·瓦勒(Philipp Wahle)亲手挑选了大约5,000名学生,然后将他们分成单个细胞。“我确信这会给我们一个大而完全独特的数据集。这对我来说是一个很好的动力,”Wahle说。这个艰苦的过程带来了新的挑战。“你需要收集几次会议以获得足够的材料进行测序运行,”负责单细胞测序团队的Christine Kocks说。它由Jonathan Alles,Salah Ayoub和Anastasiya Boltengagen组成,他们与计算科学家Nikos Karaiskos共同优化了基于液滴的测序。“所以我们必须找到一种方法来稳定细胞中的转录组,”Kocks补充道。“最后,基于他早期对C. elegans胚胎的研究,Nikolaus建议使用甲醇。”新的单细胞固定方法于2017年5月在BMC Biology上发表。
随着数据变得越来越好,Rajewsky实验室的理论物理学家和计算专家Nikos Karaiskos接受了将如此大量细胞空间映射到其精确胚胎位置的挑战。空间转录组学领域中现有的方法都不适合重建果蝇胚胎。“这是一个反复过程,过滤数据,看看里面是什么,并试图绘制它。它一路上改变了很多次,”卡拉斯科斯说。计算机实验室成员和湿实验室交换之间有很多来回,这是BIMSB的一个明确特征。“我不得不一直质疑我的工作,看看它缺乏的地方,并开发出更好的东西。”他提出了一种名为DistMap的新算法,可以将细胞的转录组数据映射到虚拟胚胎中的原始位置。
浏览未知领域
虚拟胚胎的构建使Karaiskos能够容易地预测数千个基因的表达,这是传统实验手段几乎不可能完成的任务。Philipp Wahle在Claudia Kipar的支持下,通过用传统方法在工作台上观察基因表达谱来验证这些预测:原位杂交允许用显微镜下可见的彩色染料可视化基因表达模式。“在这个阶段,单层细胞围绕整个苍蝇胚胎,”Wahle说。“这使得它非常易于访问,因此您可以将计算数据与成像进行比较。”
这是第一次可以单独观察大约6,000个胚胎细胞,评估它们的基因表达谱 - 并了解决定它们在胚胎中的行为的原因。“这项研究最重要的技术进步是,我们不会失去了解胚胎细胞协同作用所需的空间信息,”科学家说。“这真的是一个未知的领域,需要新的生物信息学方法来理解所收集的数据。这在我们的合作中非常有效,尤其是因为Rajewsky实验室的独特构成,它整合了湿实验室和计算方法。”拉杰维斯基说,一个主要的优势是,这两个群体不仅对技术感兴趣,而且还有特定的生物学问题来激励他们。“罗伯特对早期发展有着深刻的理解。我们可以进行单细胞测序运行,并具有开发工具的计算能力,这些工具可帮助我们真正了解潜在的基因调控相互作用。“
这些小组已经在计划后续项目。一个例子是在不同的时间点映射细胞以观察它们如何一起工作以形成器官和组织。另一种方法是检查映射方法是否适用于更复杂的组织。
推荐内容
-
使用酶来控制CRISPR / Cas系统 该酶也控制遗传信息转化为蛋白质
通过靶向DNA中的特定区域,CRISPR Cas系统在植物,动物和微生物的基因组编辑中被称为有希望的基因剪刀 - 甚至它们甚至可以用于纠正遗
-
多任务DNA人类基因组中的双重密码子
我们知道人类基因组是构建人体的分子教学书,但它究竟是什么功能的复杂性呢?2003年,人类基因组计划(HGP)完成,对构成完整人类基因组的30亿
-
印度载200人客机突发故障 17人重伤
印度载200人客机突发故障 17人重伤 极目新闻记者 张扬 英国BBC于5月3日报道了一起印度航班事故。印度当地时间5月1日晚上,印度香料航空
-
有机蔬菜更营养吗?真实情况是怎样
随着互联网的快速发展,我们在获取信息的时候很容易被带跑方向。有时候真相也许并不是网上说的那样,所以我们必须要有自己的判断和独立...
-
冬天给小孩穿衣服真是越多越好吗?来听听专业人士怎么说
相信很多人都被“误导”过。因为现在的网络信息非常丰富和更新迅速,还没等我们了解事情的详情,下一秒就又反转了。所以大家在获取信息...
-
十大迹象让你识别自恋狂
今天也是照常给大家说说心理方面的常识。很多人提到心理这两个字是没有概念的,以为这个东西是不需要去在意的。其实不然,随着科学知识...
-
代糖很健康,可以放心吃?需要好好科普
当我们不知道一件事真假的时候,不防多等等官方的回应。因为信息碎片化,很多小伙伴现在上网很容易只看到事情的一面就下定论,其实很多...
-
心理知识:分裂型人格障碍的症状
生活中,不管我们在跟自己独处还是跟别人相处的过程中其实我们会发现心理对一个人的影响是很大的。因此当我们发现自己有心理疾病的倾向...
-
超越XX和XY性别决定的非凡复杂性
人类在社会条件下将性和性别视为二元属性。从我们出生的那一刻起 - 甚至在此之前 - 我们被明确地标记为男孩或女孩。然而,科学指向一个
-
吃虾真的可以补肾壮阳?你知道吗
随着互联网的快速发展,我们在获取信息的时候很容易被带跑方向。有时候真相也许并不是网上说的那样,所以我们必须要有自己的判断和独立...