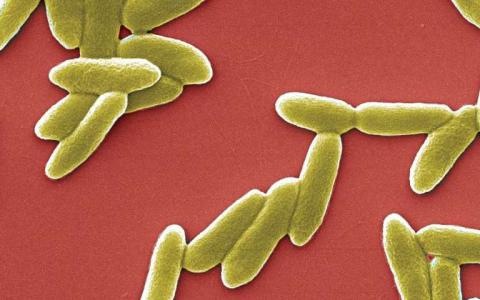
一群突变蚊子正在消灭疟疾
2015年有超过40万人死于疟疾 - 其中许多是儿童。正在释放CRISPR编辑的蚊子以期减少死亡

第二年,在布基纳法索的Bana村,一群科学家将放置多达10,000只蚊子,上面撒上荧光粉。无菌的雄性群体将代表首次向野外释放携带疟疾的转基因疟疾物种。这不仅是科学的一个里程碑,也是非洲社区参与和监管障碍的里程碑。
然而,最重要的是,这些蚊子将为最终部署强大的生物工具奠定基础,研究人员希望有朝一日能完全阻止疟疾。
总部设在伦敦帝国理工学院的目标疟疾联盟希望通过强迫昆虫对某些基因遗传的选择性偏见来彻底减少世界上传播疟疾的蚊子数量 - 这一过程被称为基因驱动。
在进化遗传学教授Austin Burt和分子寄生虫学教授Andrea Crisanti的带领下,该团队旨在改变基因遗传规则,这意味着蚊子传播给定基因的几率接近100%,而不是50-我们通常期望50。
读下一个
Twitch飘带正在打破他们的身体以获得点击和视图,Twitch飘带正在打破他们的身体以获得点击和视图
作者:CHRIS STOKEL-WALKER
只有雌性蚊子叮咬并传播疟疾。2015年12月,该研究小组在实验室的自然证明中发表了一篇论文,指出基因驱动可以降低冈比亚按蚊的女性生育能力。
近三年来,布基纳法索的发布将是他们在现实环境中技术的第一次重大测试,目的是观察改良蚊子在野外生活多久,以及他们是否加入雄性自然形成的群体在野外交配。“我们释放雄性是因为我们不想释放那些会咬人并惹恼它们并可能传播疾病的女性。我们希望尽可能多地过滤掉女性,“伯特解释说。
根据世界卫生组织(WHO)的数据,2015年有超过40万人死于疟疾,其中大多数是撒哈拉以南非洲的五岁以下儿童。
自2000年以来,将蚊帐挂在家中并向社区发出疟疾传播方式的公共卫生工作使死亡人数减半,但此后进展停滞不前。“在所有媒介传播的疾病中,疟疾在发病率和死亡率方面都是最重要的,”伯特指出。
其他几种疾病正在被转基因蚊子解决,这些蚊子已经在巴西释放以对抗寨卡病毒,而在澳大利亚则用于治疗登革热。与此同时,加利福尼亚大学的科学家正在使用被称为CRISPR / Cas9的基因“切割”工具,也被Burt的团队用来操纵蚊子基因进入阻塞疟疾。
到目前为止,还没有人成功使用转基因蚊子或基因驱动器来降低疟疾发病率,但Target Malaria认为它在布基纳法索,马里和乌干达的项目比其他任何人都更接近。“对于疟疾来说,90%的负担都在非洲,因此将重点放在撒哈拉以南非洲地区是有道理的,这三个国家都有非常好的昆虫学家,”伯特说。“将这些专业知识作为团队的一部分非常重要。”
至关重要的是,他补充说:“他们还有一个监管系统,可以考虑转基因生物”。
一年多前,布基纳法索政府批准进口基因改造的按蚊(Anopheles coluzzii)蚊子,并为他们释放了绿灯。
目标疟疾的蚊子最好是绝大多数产生雄性和少数不育雌性,从而减少总体人口规模。然后,这种“基因驱动”将通过后代传播这些趋势,摧毁负责疟疾传播的Anopheles组内的目标物种。研究人员认为,结果将在十年内显现出来。
不是每个人都喜欢永久性地改变蚊子基因的想法,而Target Malaria的工作也提出了关于实验所涉社区的道德问题。Jeantine Lunshof是一位哲学家和生物伦理学家,为麻省理工学院(MIT)的雕刻进化小组提供建议,他说,疟疾可能是唯一一种病例导致的巨大痛苦可能超过无限期繁殖基因的固有风险。
“当所有这些测试和飞行员都顺利进行时,有可能应用真正结束这些特定蚊子的基因驱动器......这可能是合理的,”她说。Lunshof与助理教授Kevin Esvelt合作,他帮助开拓了CRISPR及其在基因驱动中的应用,但他警告过任何可能在全球传播的基因驱动。
Esvelt也是“响应式科学”的强力支持者,在马萨诸塞州玛莎葡萄园岛和楠塔基特岛上与基因编辑的老鼠和莱姆病合作,促进透明度和社区反馈。
Lunshof在Esvelt的麻省理工学院实验室中引用了这一标准,称赞Target Malaria通过其利益相关方团队与当地社区的持续接触,他们将实验转化为当地语言并获得释放蚊子的知情同意。
Lunshof说,避免过去的错误至关重要,引用了全球人类遗传变异的HapMap项目,其中尼日利亚的医疗设施未兑现承诺,以换取DNA样本。
“我们必须向他们介绍这个项目,他们必须理解我们为什么这样做。我们必须寻求他们的批准,挨家挨户,“同意Jonathan Kayondo,他领导Target Malaria在乌干达的业务。
Kayondo说,当地居民和开始热情支持该项目的政治家提出的主要问题是“时间表” - 这项研究需要数年甚至数十年,人们希望“明天”获得成果。
即使得到社区的热烈欢迎,另一个问题也围绕着在相对较短的时间内从食物链中消除物种的生态影响。Burt说,影响“可能很小”,并补充说“没有掠食者专门研究这种特殊的蚊子”。他补充说,目标疟疾也只是在一种蚊子中进行基因编辑,而不是布基纳法索所有已知的疟疾传播类型。
尽管有这些假设,但在不育雄性释放后需要时间来研究对环境的影响,如果另一批蚊子(这次是肥沃的雄性)也成功,基因驱动只会继续进行。
最终,大自然本身可能会超越任何未来的Target Malaria基因驱动器。CRISPR的使用并不完美,有时单个细胞可以添加或删除随机DNA字母,这意味着修改后的代码不能正常传播。
然而,就像在抗生素中一样,自然抗性也会发生,这意味着团队必须调整他们的模型,让他们的基因在进化成为自己的过程之前有足够的时间工作。
推荐内容
-
芹菜杀精,可乐杀精,“精子危机”真的来了?具体什么情况呢
互联网时代,每个人都是信息传播者,但是我们必须清楚一点:在没有获得真正证实的消息之前,千万不能随意散播谣言,很容易造成以讹传讹...
-
心理知识:积极心理学的五大误区
社会的发展越来越快,大家现在也慢慢开始关注一个人的心理健康。因为外界事物的巨大变化,很多人跟不上变化的脚步就会产生心理落差感从...
-
心理知识:音乐为我们带来哪些功效?
随着社会压力的不断加大,人们现在把越来越多的目光放到了一个人的心理情况上。确实,每个人的抗压指数是有限的,一个平时看着正常的人...
-
克服对抗生素的抵抗力
铜绿假单胞菌可以成为引起致命感染的强大病原体,特别是在插管患者,患有囊性纤维化或严重烧伤的人群中。在细菌的天然或人类环境中存在...
-
研究重新思考人口中变异性的进化重要性
人们一直认为,人口中的变异性是人口增长和生存的关键,但新的研究质疑这种假设。哈佛John A Paulson工程与应用科学学院应用数学助理教
-
研究发现与BMI相关的非洲血统人群的人类基因组区域
包括来自国家人类基因组研究所的基因组学和全球健康研究中心的研究人员组成的一项大型研究已经确定了非洲血统人群中与体重指数(BMI)相关的
-
献血真的会“伤元气”?科学观点是说...
当我们不知道一件事真假的时候,不防多等等官方的回应。因为信息碎片化,很多小伙伴现在上网很容易只看到事情的一面就下定论,其实很多...
-
心理知识:有些事情认真了就等于“输“
今天也是照常给大家说说心理方面的常识。很多人提到心理这两个字是没有概念的,以为这个东西是不需要去在意的。其实不然,随着科学知识...
-
心理知识:男人婚后和前女友联系是什么心理
现在的人们越来越物质化了,什么都要攀比,其实生活是自己的,过得开不开心只有自己知道。有时候我们真的不需要在意别人的眼光,做自己...
-
父母喜欢可能检测到儿童对常见疾病易感性的基因检测
根据发表在4月18日网络版 儿科学 杂志上的一项新研究,父母通常愿意允许基因检测来确定他们的孩子对8种成人发病健康状况的易感性。研究小