这场改革终将让每个患者都受益
过去,药品法规和政策属于药事管理的研究范畴。大约从2006年起,学者们开始从行政管理和政治学角度研究药品监管,我有幸成为学术共同体的一员。当时,接连发生多起药品安全事件,药品审评、药价虚高问题也被广泛报道,社会反应强烈。我们在研究中逐渐形成共识——药品安全是生产出来的,也是监管出来的,强大的产业基础至关重要。
然而,谈何容易。中国制药企业数量多、规模小、创新能力弱是历史形成的,这些问题又与地方经济、医院收入相交织,解决起来十分困难。2012年我专门写了一篇学术论文,提出药品审评直接关系着企业能产什么、医院能进什么、患者能用什么、医保能报什么,因此利益和矛盾都高度集中,改革难度极大。
转折点发生在2015年8月,国务院印发《关于改革药品医疗器械审评审批制度的意见》。在此前后,监管部门、产业界、专家学者开展了深入讨论,我也参加过一些会议。我至今还在电脑里留着一张图,是药审机构对审评时滞的分析,细分每个环节,精确到天数,并针对性提出对策。大家的目标很一致,让患者吃上更加安全有效的药品。
根据我的理解,改革最初是从解决注册积压入手,提高新药和仿制药标准。所以,当时的主要举措是打击数据造假、简化审评程序以及增加技术力量。我和不少业内人士交流过,大家共同的感受是,通过徙木立信,企业有了稳定预期,敢于投入研发,申办方和监管者之间的信息也更加对称。
2016年以后,改革进一步明确了鼓励创新的思路,并出台相关制度。这种从“守底线”到“争高线”的跨越,受到广泛好评。我记得在一次论坛上,有制药企业负责人在发言时激动地说了句“药审改革,人人都爱”,全场掌声持久。我想这就是市场对有为政府的褒奖。
亲身见证这次改革,我有一个感触,有魄力的改革者把握住了新时代脉搏,干成了一件过去想干而没干成的实事。相信这场旨在催生更多安全有效药品的审评改革,终将让每个患者都受益。(讲述人:中国药品监管研究会药品治理专委会主任委员 胡颖廉 记者 陈海波采访整理)
推荐内容
-
尺寸感应蛋白控制脂肪细胞中的葡萄糖摄取和储存
爱荷华大学的研究人员发现,一种可以感知脂肪细胞肿胀的分子也可以控制一种信号通路,让脂肪细胞摄取并储存多余的葡萄糖。缺少这种蛋白质(
-
心理知识:失眠可能是心理疾病的先兆
生活中,不管我们在跟自己独处还是跟别人相处的过程中其实我们会发现心理对一个人的影响是很大的。因此当我们发现自己有心理疾病的倾向...
-
上海新增本土确诊病例2472例和无症状感染者16983例
中新网4月25日电 据上海市卫健委微信公众号消息,2022年4月24日0—24时,上海市新增本土新冠肺炎确诊病例2472例和无症状感染者16983
-
国家卫健委:5月9日新增新冠肺炎本土确诊病例349例 本土无症状感
据国家卫健委网站消息,5月9日0—24时,31个省(自治区、直辖市)和新疆生产建设兵团报告新增确诊病例357例。其中境外输入病例8例(广西3
-
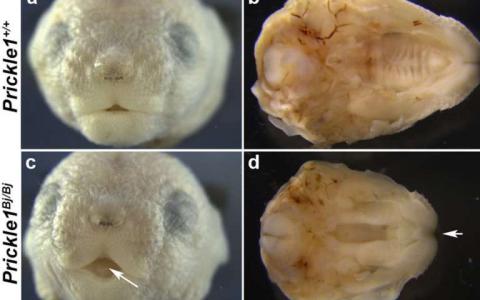
Prickle1基因调节新动物模型中额骨成骨细胞的分化
由于颅骨原基(发育中的头骨)中成骨细胞的迁移和分化缺陷,囟门增大,前额骨小,可导致机械损伤的颅骨。所述的Wnt 平面细胞极性的信号传导
-
“日行万步”真的有益于健康吗?事实又是什么?
面对流言,希望我们第一时间想到的是寻找官方回应。而不是着急着把流言传播出去,毕竟现在网络相关的法律法规都出台了,网络上传播谣言...
-
心理知识:怎样消除自卑心理
现在的人们越来越物质化了,什么都要攀比,其实生活是自己的,过得开不开心只有自己知道。有时候我们真的不需要在意别人的眼光,做自己...
-
合成生物学时代就在这里 - 我们如何才能充分利用它
我们正在进入定向设计的时代,我们将扩展有限的观念,即生物学只是生命和生物的研究,并将生物学视为最终的分布式制造平台(正如斯坦福生物
-
心理知识:吵架后男人冷战是什么心理
社会的发展越来越快,大家现在也慢慢开始关注一个人的心理健康。因为外界事物的巨大变化,很多人跟不上变化的脚步就会产生心理落差感从...
-
在美国细菌中具有共利斯汀抗性基因的第二例
美国爱荷华州北自由市JMI实验室的 Mariana Castanheira博士领导的科学家小组第二次在美国人类中检测到了具有大肠菌素抗性基因mcr-1 的大