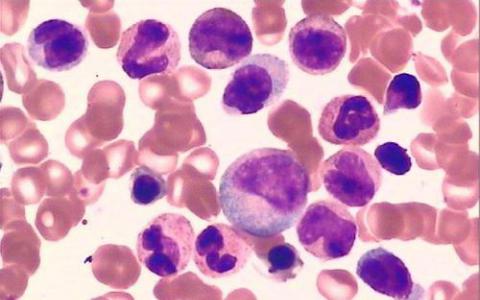
新工具为活细胞中的蛋白质浓缩提供了亮点
利用光来操纵活细胞内物质的工具已经开始解释蛋白质如何组装成不同的液体和凝胶状固体状态,这是理解许多关键细胞操作的关键。复杂的奇迹,细胞同时存在数千个化学反应。一些反应发生在专门的隔室内,称为细胞器。然而,某些细胞器缺少任何膜以使其自身脱离细胞内漂浮的其余物质。这些无膜细胞器以某种形式存在于水,蛋白质,核酸和其他分子的细胞海洋中的独立结构中。
普林斯顿大学的科学家们已经开发出一种新工具,称为optoDroplet,它提供了前所未有的操作和理解化学的途径,使无膜细胞器能够发挥作用。
“这种optoDroplet工具开始允许我们剖析管理无膜细胞器自组装的物理和化学规则,”普林斯顿化学和生物工程助理教授,在线发表论文的高级作者Clifford Brangwynne说。在细胞上12月29日“这个过程背后的基本机制是非常知之甚少,如果我们就可以得到一个处理,有可能发展的干预和治疗方法具有毁灭性蛋白聚集有关的疾病,如ALS希望。 “
先前的研究已经证明,无膜细胞器通过称为相变的过程在细胞内组装:熟悉的相变的实例包括水蒸气冷凝成露珠或液态水冷冻成固体冰。Brangwynne及其同事在过去几年的研究表明,改变某些蛋白质的浓度或改变其结构似乎会引发相变,使蛋白质凝结成液滴状细胞器。
然而,迄今为止,大多数研究都使用在试管中研究的纯化蛋白质,研究人员几乎没有方法研究作为活细胞的狂热发电机的相变。OptoDroplets将帮助科学家了解相变何时出错,产生类固体凝胶和与阿尔茨海默氏症和肌萎缩侧索硬化症(ALS)等疾病有关的蛋白质结晶聚集体。
OptoDroplet依赖于一种称为光遗传学的技术,涉及蛋白质,其行为可以通过暴露于光线而改变。(细胞主要是水,因此基本上是透明的。)研究人员表明,它们可以通过开启光活化蛋白诱导相变并产生无膜细胞器。它们还可以通过简单地关闭灯来撤消转换。增加光强度和蛋白质浓度使研究人员能够进一步控制转变。通过改变这些输入,他们可以确定何时形成浓缩的液体蛋白质液滴,以及可能与疾病相关的固体状蛋白质聚集体。
“OptoDroplet为我们提供了一定程度的控制,我们可以使用它来精确地绘制我们称之为活细胞中相图的图,”Brangwynne说。“通过这种方式,我们开始了解细胞如何利用它们的天然机器通过这种细胞内相图来组装不同类型的细胞器。”
该论文的第一作者是Yongdae Shin,他是Brangwynne的Soft Living Matter Group的博士后研究员,是普林斯顿大学化学与生物工程系的一部分。共同作者机械和航空航天工程系的Joel Berry和Mikko Haataja帮助开发了用于理解细胞内相行为的数学模型,而分子生物学系的Nicole Pannucci和Jared Toettcher是光遗传学的专家,并帮助指导了分子设计。 optoDroplet蛋白质。这项工作部分得到了美国国立卫生研究院和国家科学基金会的支持。
利用小鼠和人类细胞,研究小组在一个基因中拼接了一种光敏蛋白,这种蛋白来自一种称为小鼠耳水芹(或拟南芥)的植物,这是一种白菜和芥菜的亲戚,是遗传学研究的支柱。蓝光暴露导致蛋白质自我关联,自我碾压。
光敏标签融合到被认为能够驱动活细胞相变的蛋白质成分中。利用光线,研究人员发现它们可以诱导蛋白质蜷缩,模仿细胞中自然发生的凝结过程。“使用水蒸气的类比,你可以想到我们用激光来局部改变某些空气区域的温度,以便水滴凝结出来,”Brangwynne说。
该团队反复提示蛋白质凝结,然后通过打开和关闭灯光来溶解。即使经过多次循环,该过程也证明是完全可逆的。然而,在高强度光或高浓度蛋白质的情况下,研究人员创造了半固体凝胶。这些凝胶最初是可逆的,但随着时间的推移,它们凝固形成不可逆的块状聚集体,类似于某些疾病中发现的那些。
“我们已经向optoDroplet展示了我们可以轻松组装和拆卸相分离液体,它们似乎不会对电池造成任何问题,”Brangwynne说。“但凝胶状组装似乎更成问题,因为在很多循环中,它们会发展成持久的聚集体,细胞不再能够处理这种聚集体,并且可能开始破坏健康的生物过程。”
一个例子是称为FUS的蛋白质。FUS蛋白对细胞的操作至关重要; 它有助于产生其他蛋白质并修复受损的DNA。但是大量的基因突变可能导致FUS蛋白变得过于粘稠,导致肌萎缩侧索硬化症,也被称为卢格里格病。一种神经系统疾病,患者失去了自愿控制肌肉的能力,ALS的特征是神经细胞中积聚的蛋白质团块。这些团块可能源于病毒聚集的FUS或其他蛋白质,而不是像动态液滴一样。亨廷顿氏病和阿尔茨海默氏症也涉及堵塞细胞的蛋白质块,再次表明细胞中的异常相变与这些条件密切相关。
Edward Lemke是德国海德堡欧洲分子生物学实验室的研究员,他没有参与细胞研究,他指出了optoDroplet的前景。
“optoDroplet靶向的蛋白质是相分离蛋白质的重要组成部分,其中许多蛋白质也与臭名昭着的疾病有关,”Lemke说。“optoDroplet系统能够以微创和高度可控的方式调节细胞内这些蛋白质的状态,因此它可以提供有关它们如何实现其功能的新见解。”
Brangwynne及其同事期待继续尝试使用optoDroplet来更好地了解细胞的复杂行为。“这是我们正在做的基础科学,回答有关细胞相变的基本问题,”Brangwynne说。“但我们希望这些见解不仅能揭示健康细胞的运作方式,还能揭示它们如何变得患病,最终可能治愈。”
推荐内容
-
人民币兑美元升破6.7关口还会继续涨吗 人民币升值的利弊
人民币兑美元升破6 7关口还会继续涨吗?笔者认为,随着中国在控制疫情、企业复工和外贸方面做得很扎实,基本经济数据有复苏迹象,未来人民币
-
10月26日俄罗斯疫情最新数据公布 俄罗斯新增36446例确诊病例
你知道俄罗斯目前疫情什么情况吗?俄罗斯疫情有多少人确诊了?据消息显示,俄罗斯新增36446例确诊病例,新增1106例死亡病例。俄罗斯卫星通讯
-
方洋洋为什么流过产长什么样子照片 方洋洋案为什么判这么轻更
【摘要】自从方洋洋被婆家认为不能生育后,两年来,她熬过了很多个被虐打、饿饭和挨冻的日子,但没熬过2019年第一个月的最后一天。在整个村
-
9月13日张家界长沙株洲疫情最新数据公布 湖南昨日报告新增新型
温馨提示:一旦出现发热、干咳、乏力、鼻塞、流涕、咽痛、嗅觉味觉减退、结膜炎、肌痛和腹泻等症状,应及时按规范程序就诊,并主动告知1...
-
哈利波特手游冬季版最新彩蛋福利来袭 哈利波特魔法觉醒12月新
今天一则关于哈利波特手游冬季版最新彩蛋福利来袭相关话题引起了网上热议,想必大家对于哈利波特手游冬季版最新彩蛋福利来袭一事是非常...
-
香港疫情10月9日最新消息 新增确诊病例8例其中3人为同一酒店员工
今天是10月9日,也是假日结束的第一天,今天的香港疫情怎么样?根据香港特区政府卫生署10月9日通报最新消息获悉,昨日香港新增确诊病例8例,
-
超越基因来解释血细胞的命运
科学家经常谈论细胞命运和控制基因表达机制(转录因子,染色质重塑等)的承诺。但是,通过研究罕见的遗传性血液病Diamond-Blackfan贫血症(DBA
-
8月16日浙江疫情最新实时数据消息公布 浙江昨日新增5例境外
浙江8月15日新增5例境外输入确诊病例,为弘进轮船员。那么,对于浙江疫情的这个话题,今天的你是否也在关注着?具体什么情况?下面跟小编一起
-
全国国内疫情10月10日最新消息 新增确诊病例15例均为境外输入病例
今天是10月10日,今天的国内疫情情况如何?据悉,昨日全国新增确诊病例15例,均为境外输入病例,无新增死亡病例,无新增疑似病例。下面我们
-
9月17日云南德宏州疫情最新数据公布 云南昨日新增本土确诊1例
想必大家都知道,云南省,简称云或滇,中国23个省之一,位于西南地区,省会昆明。那么,你知道目前云南疫情什么情况吗?@云南发布 微博消息