CRISPR指导RNA结构的修饰防止靶细胞中的免疫应答
CRISPR介导的基因组编辑已成为各种生物体中疾病建模的有力工具,并且正在开发用于临床应用。由重组Cas9蛋白和体外转录(IVT)指导RNA复合物组成的预组装的Cas9核糖核蛋白(RNP)可以被递送到细胞中,而没有外来DNA整合到宿主基因组中的风险并且具有更少的脱靶效应。然而,在今天发表在基因组研究中的一项研究中,科学家发现体外转录的gRNA含有5'三磷酸(5'ppp)部分,激活人体细胞的免疫反应,导致细胞死亡。
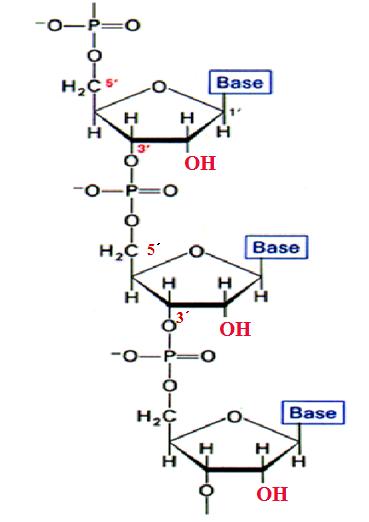
“CRISPR-Cas9 RNPs现在广泛用于生物医学研究,并在治疗性基因组编辑方面具有前景”,来自基础科学研究所(韩国首尔)的相应作者Jin-Soo Kim说。因此,将该技术从生物医学应用转化为临床应用需要对潜在有害的宿主反应进行彻底调查。
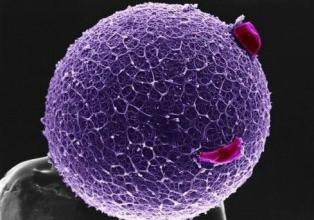
在这项研究中,研究人员生成并转染了与纯化的Cas9复合的IVT gRNA,进入人宫颈癌细胞(HeLa)和小鼠胚胎成纤维细胞。在这些细胞中,5'ppp gRNA引发I型干扰素介导的免疫应答,以及干扰素激活的抗病毒效应蛋白(例如DDX58)的表达增加,导致细胞死亡。
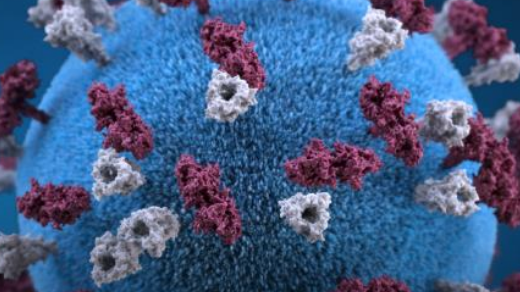
此外,该研究证明了5'ppp gRNA对人T细胞的细胞毒性作用。“T细胞中的基因组编辑在治疗癌症和HIV感染的细胞疗法中具有很大的前景.T细胞对gRNA中的5'三磷酸基团极为敏感”Kim说。T细胞表面受体CCR5参与HIV病毒进入,因此是抗HIV治疗的有希望的靶标。Kim等人。表明用磷酸酶预处理IVT gRNA,去除了5'ppp并显着降低了T细胞宿主的免疫反应和细胞毒性。磷酸酶处理的IVT gRNA显示出针对CCR5的突变效率增加,导致该HIV辅助受体的细胞表面呈递显着降低。
该研究通过免疫激活CRISPR-Cas9或Cpf1核糖核蛋白复合物中的IVT gRNA来阐明对人体细胞的细胞毒性作用,并提供一种新的方法来预防宿主免疫应答,同时保持高突变效率,朝着CRISPR介导的基因组编辑的有效治疗应用。
推荐内容
-
2020年最受欢迎的奶粉品牌有哪些,全新婴儿奶粉排行榜汇总
妈妈们给宝宝选择奶粉的时候,我发现了一个奇怪的现象,不少妈妈在选择的奶粉的时候喜欢参考一下奶粉排行榜,这不,新的一年,不少妈妈私
-
了解细胞诱捕门的锁定可能会导致更好的疾病治疗
一个研究小组在两年前宣布了一种特洛伊木马进入细胞而不伤害它的方法,现在已经发现了对细胞陷阱门的锁定。这项由Jean-Philippe Pellois博
-
8家医疗技术公司从FDA获得阿片类药物设备
FDA已从250多名申请人中挑选了8家医疗技术公司,作为其创新挑战赛的获奖者,该挑战 由CDRH于5月推出, 旨在激励医疗技术解决方案的发展,
-
头颈部黑色素瘤在儿童和年轻人中的发病率上升了51%
根据圣路易斯大学的研究,美国和加拿大儿科、青少年和年轻成人人群中的头颈部黑色素瘤从1995年到2014年增加了51 1%。 在美国,黑色素...
-
大健康+信息科技高峰论坛 康加董事长牟贵先三个维度剑论主题
引题:解锁产业发展动因 促进产业融合发展由北京市海淀区大健康产业联合会主办的大健康+信息科技高峰论坛于2018年12月22日在海淀文化核心
-
一种快速检测腹腔疾病抗体的新诊断方法
点对点(POC)检测是一个快速发展的领域,它将医学检测从中心实验室带到患者接受治疗的地方。 来自赫尔辛基大学的研究人员开发了一种新的...
-
默克公司与Themis合作开发基于麻疹病毒载体的疫苗
默克公司将与Themis Bioscience合作,通过奥地利生物技术公司与一家主要生物制药公司的首次合作,基于Themis基于麻疹病毒载体的平台开发候
-
教你42种适合小孩做的甜品及哪些饮食习惯会致使女性不孕
儿童的饮食与成人的饮食不同。儿童的抵抗力较小,因此饮食应更卫生。儿童饮食的味道也清淡而甜。他们喜欢它,尤其是在夏天来临时,糖果...
-
女性罹患慢性阻塞性肺疾病的风险较高
瑞典隆德大学的研究人员通过一种新的诊断方法已经表明,女性患慢性阻塞性肺疾病的风险可能是男性的两倍。这意味着女性可能是患此病的独...
-
科学家开始揭示蛋白质tau如何从可溶性液态转变为固态纤维缠结
虽然很多关于阿尔茨海默病的事情仍然是一个谜,科学家确实知道,这种疾病的进展部分涉及一种叫做tau的正常蛋白质,聚集在脑细胞内形成绳状