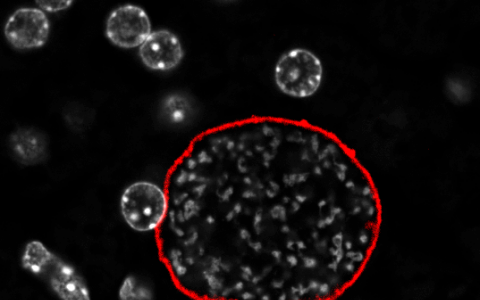
生物学家发现源促进肿瘤细胞药物敏感性的源头
dna有害,或者“银两”,组成最广泛使用的抗癌药物。然而他们治疗成功限制了药物resistance-either出现在癌症细胞的疾病发作或治疗期间出现。现在,圣地亚哥加利福尼亚大学的生物学家发现了一个新的re-sensitizing方式人类肿瘤细胞耐药的效力的银两。
加州大学圣地亚哥分校项目科学家满清李教授迈克尔·大卫和他们的同事描述在10月29日在《自然结构和分子生物学如何人类基因被称为Schlafen 11控制肿瘤细胞的敏感性银两。因此,他们的研究可能为新策略来克服化疗耐药的方法。
大卫•施瓦兹,1998年在加州大学圣地亚哥分校生物科学教授斯蒂芬•亨德里克的实验室发现了第一Schlafen基因在小鼠体内。他的德语词命名为睡眠因为基因的蛋白质产品可以导致细胞停止分裂。2012年大卫和李检查Schlafen 11日人类遗传与最初的发现,发现了艾滋病病毒复制的作用。他们发现人类Schlafen 11基因编码一种蛋白质,这种蛋白质阻碍了艾滋病病毒在感染人类细胞的复制通过阻断病毒蛋白的合成没有抑制宿主细胞合成蛋白质的总体能力。
在新的后续研究聚焦于肿瘤,研究人员发现了一个类似的选择性Schlafen 11对DNA损伤反应的两个“主控制器”:ATM和ATR,蛋白质的丝氨酸/苏氨酸激酶闻名在DNA损伤修复中心的角色。
“我们发现,如果你暴露的细胞有Schlafen 11到DNA损伤因子,Schlafen 11个蛋白被激活和抑制的合成ATM和ATR-that就是杀死肿瘤细胞,”大卫说,生物科学部分分子生物学教授和加州大学圣地亚哥分校穆尔斯癌症中心。“细胞中不表达Schlafen 11日你不的ATM / ATR和差别得到这对这些本质上允许肿瘤细胞生存。”
探索深入Schlafen 11如何运作机制在分子水平上,研究人员发现,激活Schlafen 11蛋白裂解转移rna的特定子集,这额外的茎环结构特征。这些图示不是经典的“三叶草”类型的设计,而是有独特的“四叶苜蓿”设计,区分标志,可能作为Schlafen 11目标点。在这些影响都是转移rna氨基酸白氨酸和丝氨酸。其中一个特别“tRNA-Leu-TAA”,是极低丰度的细胞,但相应的密码子使用频率高的ATM和ATR的基因。当这个tRNA被劈理、ATM和ATR是最敏感的目标蛋白质合成抑制Schlafen 11。
进一步的调查显示,大部分的基因在DNA损伤修复显示类似的扭曲的转移核糖核酸对tRNA-Leu-TAA像艾滋病一样使用。然后研究人员开发出一种新技术来re-sensitize Schlafen 11-deficient肿瘤细胞直接针对tRNA-Leu-TAA药物。这种干预会影响整个DNA损伤修复途径——包括ATM和ATR-rather比抑制一个特定的组件的功能。他们说,这种策略可能会有巨大的潜力在临床癌症治疗和解决耐药性的挑战。
研究合著者Jean王名誉教授在加州大学圣地亚哥分校医学院的,说知道癌细胞逃脱死亡时他们的DNA受损将创建新的策略来增强癌细胞通过化疗杀死。
“这些结果表明两种方法来提高能损伤dna药物杀死癌细胞的增加1)ATR抑制剂或2)tRNA抑制剂,”王说。“意义的论文也基本研究DNA损伤反应,因为它第一次表明,监管的图示决定当一个受损的细胞生存或死亡。”
除了与DNA损伤和癌症,大卫指出,新的结果携带潜在应用以来,免疫学和病毒学Schlafen 11也在背后的基本机制在抗艾滋病病毒的过程和可能与其他病毒。
推荐内容
-
科普夏季饮食以清淡养胃为宜及一星期3顿鱼虾可以更健康
天气越来越热。中医医生介绍,夏季开始烈日炎炎,人体新陈代谢旺盛,阳气外发,伏阴于内,因此,在炎热的夏季要注意保护体内阳气,避免...
-
林承纬是谁什么职业个人资料简介 春日迟迟再出发设计总监林承
【导读】林承纬是谁?据消息显示,林承纬,39岁,是台湾人,与前妻是初恋在一起13年才结婚,结婚生子后感情慢慢淡了。2014年结婚后于2019年
-
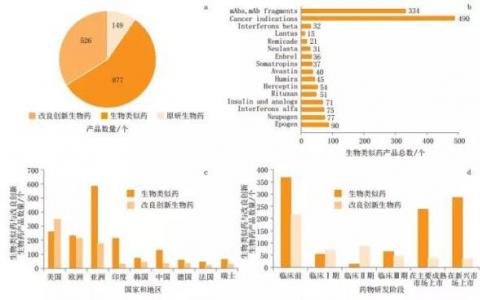
生物类似药与创新改良生物药的定义和产业态势
伴随监管政策法规的日趋成熟以及各利益相关方对生物类似药与改良创新生物药的逐渐接受,对生物类似药与改良创新生物药这2类生物药的产业态
-
岐黄名医说丨中医“妙方”,带你逃离“眼疾”
岐黄名医说丨中医“妙方”,带你逃离“眼疾” 记者 焦守广 通讯员 马昕 杨小荷眼睛是心灵的窗户,是人们认识世界、感悟自然的...
-
国产光刻设备能刻芯片?技术上差很远? 真的假的?
国产光刻设备能刻芯片?技术上差很远? 真的假的?流量为王的时代,消息的传播方式多种多样,但其中很多消息还没被证实真实性就大范围传播
-
别把癌症当鼻炎!鼻咽癌来袭时,身体或会给你5个“暗示”
别把癌症当鼻炎!鼻咽癌来袭时,身体或会给你5个“暗示” 有一种粗心叫做把癌症当成了鼻炎!近日,据《江西都市现场》报道,前几个...
-
主人拍到猫咪捕捉老鼠现场 高能解说笑喷网友
笑喷!主人拍到猫咪捕捉老鼠现场 高能解说笑喷网友。你看过老鼠和猫相亲相爱的画面吗?那是不可能的,接下来就让小编带你去看看一段猫戏老
-
生长因子显著影响脂肪和碳水化合物代谢
一种因其在癌症中的作用而被研究的蛋白质,可能代表一种令人惊讶的代谢综合征和相关疾病(如2型糖尿病和脂肪肝)的新疗法。在肥胖小鼠模型研
-
研究人员发现新类型的干细胞状态
这不是脂肪的含量,但储存脂肪的能力在正确的位置,这相当于人类新陈代谢的健康有益。在某种程度上,会发生这样的情况,新的脂肪细胞必须随需应
-
代谢直接影响疟疾发病的可能性
传染病的进展和发展不仅直接依赖于感染因子的特征,而且还依赖于宿主的遗传特征,这也决定了感染的效率。来自Instituto de Medicina Mol