对速度的需求使基因组编辑有效
莱斯大学的研究人员开发了一种计算模型来量化CRISPR-Cas9蛋白质发现其基因组编辑目标的机制。化学和化学与生物分子工程的莱斯教授阿纳托利科洛梅斯基和校友阿列克谢希弗特改编了他们之前开发的系统,以展示蛋白质如何找到它们的生物靶标。他们希望修改后的模型能够帮助解开CRISPR的其余奥秘。
在其天然状态下,CRISPR代表“聚集有规律的间隔短回文重复序列”,是细菌保护自身免受病毒感染的生物学机制。这些细菌包含了一份外国DNA,并建立了所有入侵者的记录。它们在检测到新入侵者时引用该记录并使用它来销毁它们。
近年来,研究人员已开始调整基因组编辑中使用的机制,该机制有可能治愈疾病并增强包括人类在内的生物体。但一个绊脚石的风险是CRISPR-Cas9蛋白(利用CRISPR方法的系统之一)将切割并替换错误的靶序列,引入突变。
生物物理杂志中描述的Rice模型发现,当允许这些脱靶编辑发生时,CRISPR-Cas9可能更有效地定位良好的靶标,因为蛋白质不会浪费时间与脱靶相关以继续搜索。
Kolomeisky说,这可能是也可能不是一件好事,但它肯定值得研究。“错误率(脱靶率)有时是10-20%,”他说。“我们有两个想法:一个是病毒变异非常快,也许细菌试图削减只是稍微突变的目标,以便更灵活。另一个是有蛋白质可以纠正错误,所以如果错误的削减并不多,系统可以容忍它们。
Kolomeisky说,他的模型是一个简单的步骤,可以找出CRISPR编辑的动态。“CRISPR-Cas9是最受欢迎的变种,因为它只含有一种蛋白质,在生物学上更容易使用,”他说。
莱斯实验室开发了其原始模型,以了解蛋白质如何沿着DNA滑动以找到目标并触发基因转录等过程。Kolomeisky指出,CRISPR先驱Jennifer Doudna发现CRISPR-Cas9不会以同样的方式寻找。“她发现它不会在DNA的任何地方滑动,”他说。
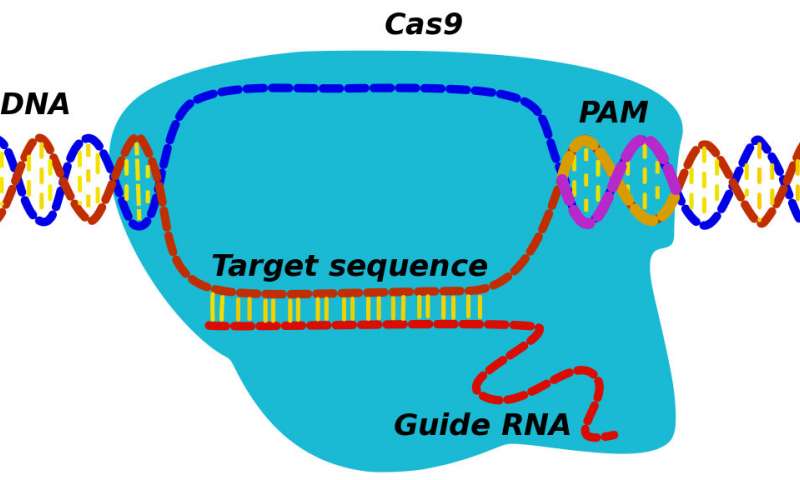
相反,根据Doudna和她的团队,蛋白质最初识别三核苷酸PAM(用于原型间隔相邻基序)序列,标记潜在靶标的位置。“CRISPR发现并结合PAM,然后其相关的RNA探索相邻的DNA,看看它是否是目标,”Kolomeisky说。“如果是的话,蛋白质会开始减少。如果没有,它会解除分离,并在其他地方寻找。”
在Doudna随后删除PAM序列的实验中,CRISPR-Cas9蛋白根本找不到它们的靶标。因此,PAMs具有重要作用,而不仅仅是一个通用的间隔物,他说。“一旦我读到这篇文章,我就知道我们也可以在这里使用我们的模型。”
理论模型着眼于第一次通过过程 - 当系统超过物理或化学阈值时发生的那些过程,例如找到相关的PAM来跟踪插入到细胞中的CRISPR-Cas9蛋白,因为它们首先调查PAM序列,然后结合到PAMs,搜索与Cas9 RNA相匹配的DNA靶标。
他们发现,通过与“错误的”DNA分离而避免脱靶的切割的CRISPR比需要更长时间定位的CRISPR比仅仅切断目标的更长。“走向错误的PAM需要时间,”Kolomeisky说。“我们的计算结果表明,当有时候切入错误的地方时,CRISPR可以更快找到真正的目标。进入正确目标的部分可能会更小,但最终会削减它们。
“这是一个简单的模型,完全可以解决,”Kolomeisky说。“如果有人想测试,该模型可以提供具体的预测,并在某些情况下提供应该观察的趋势。” 模型中遗漏的是能够看到RNA密钥是否同时识别其靶标同时与DNA结合 - 或者依次与核苷酸核苷酸结合。
“关于CRISPR的最令人印象深刻的事情不是在细菌中发现免疫系统,而是在生物技术方面创造了一场革命,因为这意味着在任何细胞中我们都可以在特定位置切割任何DNA,非常精确,”科洛梅斯基说。“我希望我们的工作能够激发更多的基础研究,因为我非常喜欢CRISPR方法。但是当人们应用它而不理解它在分子水平上如何工作时,我感到不快乐。”
Shvets现在是麻省理工学院的博士后研究员。Kolomeisky是化学和化学与生物分子工程的教授。
推荐内容
-
净化细胞治疗疾病
各种细胞疗法涉及将特定细胞类型注射到患者体内。这些包括,例如,骨髓移植和某些类型的免疫疗法,这些疗法使用T细胞(参与免疫的白细胞)来
-
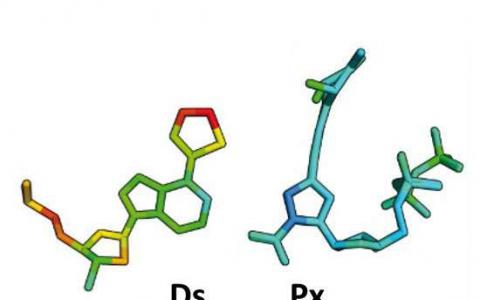
研究人员创造了新的 字母 以增强DNA功能
就像字母串在一起形成单词一样,我们的DNA也通过字母串在一起编码蛋白质。遗传字母表只包含4个自然字母--A,C,G和T,它们可以生成蛋白质的
-
操场埋尸案最新消息:埋尸案推土师傅是生是死找到了吗?操场埋尸
埋葬邓世平的司机是谁?新晃埋尸案推土机师傅失踪找到了吗?而随着操场埋尸案侦办细节的曝光,想必现在大家最关注的话题莫过于当初新晃埋...
-
部分援沪医疗队启程离沪!上海多家方舱医院休舱
部分援沪医疗队启程离沪!上海多家方舱医院休舱 人民网上海5月9日电 (唐小丽)5月9日上午举行的上海市疫情防控工作新闻发布会上,上海
-
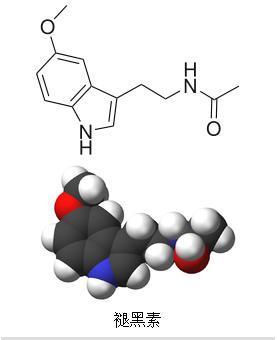
科学家们开发了两种对睡眠和其他生物过程至关重要的褪黑激素受体
一个国际研究团队在能源部的SLAC国家加速器实验室使用X射线激光器创建了两个褪黑素受体的第一个详细地图,这些受体告诉我们的身体什么时候
-
新型疫苗策略可针对基孔肯雅病毒提供快速和长期的保护
基孔肯雅热病毒(CHIKV)通过蚊子传播,并引起发烧和关节痛,有时甚至变得严重且致残。该病毒的爆发已经在非洲,亚洲和欧洲发生,2013年末,
-
「睡眠水」真的能治疗失眠吗?科学观点是说...
当我们不知道一件事真假的时候,不防多等等官方的回应。因为信息碎片化,很多小伙伴现在上网很容易只看到事情的一面就下定论,其实很多...