使用DLS和机器学习测试治疗性蛋白质的稳定性
来自不同领域的PIPPI科学家正在开发方法,工具和数据库,以指导合理配制强大的蛋白质疗法。他们的总体目标是开发一个数据库来指导产品配方的开发。
动态光散射(DLS)是用于高通量聚集筛选的主要生物物理技术,PIPPI广泛使用。
在接受News-Medical和Life Sciences的采访时,Lorenzo Gentiluomo详述了用于评估稳定性的各种DLS方法,包括一些新颖的应用。他还解释了DLS等高吞吐量技术的发展如何极大地增加了查找数据模式的机会以及机器学习在此过程中的作用。
你能解释光散射在PIPPI研究中的作用吗?
PIPPI联盟正在编制一个包含18种代表性蛋白质的数据库,以表征成功配方开发的关键属性。它将包括24种配方的基本特征,作为盐浓度和pH的函数。此外,一些配方将进行更深入的分子表征,其中蛋白质的结构特性与溶液行为有关。
这项工作的一个重要部分是使用动态光散射(DLS)和静态光散射(SLS)研究蛋白质 - 蛋白质相互作用。我们使用Wyatt的DynaPro Plate Reader测量蛋白质相互作用,该读数器具有温度控制的微孔板。
DynaPro Plate Reader可以对蛋白质的大小,分子量和相互作用进行DLS和SLS测量,从而很好地理解蛋白质制剂的物理稳定性。可以确定尺寸,分子量,多分散性,粘度和相互作用参数,然后确定配方条件和温度。
我们通过遵循平移扩散系数k D的浓度依赖性,使用DLS测量蛋白质 - 蛋白质相互作用。通过同时测量SLS,我们还可以确定成对分子间相互作用的强度,即第二维里系数A 2或B 22。这提供了一种对胶体稳定性配方进行分级的好方法。
有两种理论用于描述成对蛋白质 - 蛋白质分子间相互作用。我更喜欢使用接近能量框架,即反映距离依赖性的势能差异。增加离子强度可以屏蔽电荷 - 电荷相互作用,并且应该提供更快的聚集,因为分子更容易相互作用。
扩散相互作用参数k D已经表明它是配方的关键生物物理特性; 它不仅是蛋白质相互作用的衡量标准。最近对抗体制剂的k D测量揭示了k D与制剂的表观溶解度,热稳定性,流变学和静电性质之间的关系。
您对蛋白质的哪些特性有所描述?
我们将18种蛋白质的24种制剂表征为pH和离子强度的函数,然后应用计算屏幕,计算具有相对分子描述符的24种不同制剂中的每一种中蛋白质的3D结构。从筛选中,我们收集了一系列产出。一些来自通过DLS进行的应力测定以及通过与多角度光散射(SEC-MALS)结合的尺寸排阻色谱法。
一个重要的参数是暴露于热应力时的聚集模式,因为这可以使我们更好地理解配方开发过程中解决问题的需要。为了评估蛋白质的热稳定性,测量聚集作为pH和离子强度的函数。使用相同浓度的缓冲液,但加入不同量的盐以改变离子强度。通过SLS测量聚集发生的温度(T agg)。应该注意的是,T agg并不总是与结构稳定性相关,因为聚集可以在蛋白质开始展开之前发生(由内在荧光确定)。
聚合模式可以告诉您蛋白质的行为方式。例如,如果聚集在两个步骤中发生,其间存在平台,这表明蛋白质最可能在单体和复合物之间具有平衡 - 它不仅与温度有关。
我们还使用光散射来评估蛋白质 - 蛋白质相互作用以及它如何随着不同的离子强度而变化。k D曲线的形状通常是pH的函数,并且通过添加盐而变平。当我看到这样的扁平化时,我知道聚集是由疏水或偶极相互作用引起的。
在某些情况下,尺寸排阻色谱的结果和来自原始样品的DLS的结果不一致。重要的是要将两种测量结果都考虑在内,以便对配方有一个很好的理解。
您如何使用此类信息评估配方?
一旦我们测量了各种输出,我们就可以使用同源建模将它们与结构信息进行比较。通过这种方式,我们可以找出表面变化的原因。如果我们发现k D对于不同的抗体以某种方式趋势,我们可以评估这是否是由于疏水补丁引起的。
然而,我们的最终目标是使用分子描述符来尝试生成可用于预测特定蛋白质结果的全局算法。我们的系统方法应该有助于指出哪些是蛋白质配方的关键生物物理特性和数据挖掘技术的应用。我们确实相信,我们的数据库可以快速,节省成本地评估发展潜力。
在筛选期间,使用DynaPro平板读数器和SEC-MALS收集总数据点的75%,其中后者包括或连接到Wyatt miniDAWN MALS仪器和Wyatt Optilab差示折射计的HPLC装置。因此,您可以看到光散射对蛋白质配方开发的贡献非常显着。
您用于研究蛋白质稳定性的新方法是什么?
我们使用DynaPro Plate Reader以新颖的方式研究单克隆抗体的物理稳定性。
首先,将抗体在变性剂盐酸胍中孵育,这允许我们使用等温化学变性技术(ICD)通过内在蛋白质荧光跟踪结构的扰动。然后,我们应用了一种新方法,即'变性剂稀释液(DFD)
通过随后用缓冲液稀释变性溶液,我们可以评估物理稳定性的水平。如果物理稳定性较低,最终解决方案将具有比较高的聚集体或更多聚集体。当我们将DLS测量与SEC-MALS分析进行比较时,我们发现较高的流体动力学半径与更多的聚集体正相关。由于动态光散射对聚集检测非常敏感,并且(与SEC-MALS不同)是一种高通量技术,因此它为这种研究中的评估提供了理想的方法。
使用两种不同的缓冲液 - 组氨酸和柠檬酸盐 - 但相同的pH,由ICD评估的构象稳定性非常相似。然而,使用DFD我们能够通过DLS和流体动力学半径区分最终稳定性,这与胶体稳定性有关。这个值就是我们只需要一个值,即流体动力学半径,就可以得到全貌。
从我们的观点来看,在从不同浓度的变性剂稀释后使用DynaPro Plate Reader跟踪聚集是一种非常有前途的方法,用于探测蛋白质在不同配方中的物理稳定性。
DFD方法是等温的,因此我们避免了样品加热引起的所有问题,例如,可能发生的缓冲液pH的变化。它只需要非常短的测量时间,因此具有很小的缩小和自动化潜力。而且,它可以区分重叠的ICD曲线。这意味着您可以通过量化其胶体稳定性而无需额外努力来区分具有相同构象稳定性的两种制剂。
机器学习算法如何适应?
机器学习算法是人工神经网络在蛋白质制剂开发中的应用。人工神经网络具有处理药物开发过程中经常遇到的高度神经线性问题的能力。
我们开发了一种人工神经网络算法,以提高我们对蛋白质溶液行为的理解。我们将数据提供给算法,并预测结果。例如,如果我们输入有关主要序列和配方的信息,我们将恢复聚合的温度。
因此,人工神经网络代表了经典统计方法的一个非常有趣的替代方案。当应用于高度非线性的数据集时,它可以相当成功,并且这种数据集是制药开发中最常遇到的。
它可以应用于简单地基于氨基酸组成优化生物制剂。这将允许选择具有良好预测的T m,T agg,k D的蛋白质结构,并且在某些情况下单体保留,甚至在它们在细胞中表达之前。
使用各种模型,我们验证了算法,发现T agg的预测非常准确。它还准确地预测k D是阳性还是阴性(即,蛋白质是自排斥的或自我吸引的,分别对应于胶体稳定性或不稳定性)。回归问题很难解决,所以我们关注的是k D的符号而不是推导出一个定量值。
我们还对预测应力后的单体保留或损失感兴趣。单体保留的预测,即在应力下不聚集或碎裂的材料的比例,也是相当准确的。
大量的背景噪音意味着很难区分不同的配方。但是,我们可以预测一种蛋白质是否比另一种蛋白质更稳定。由于这是从初级序列预测的,因此我们可以对候选生物制剂的稳定性进行相对可靠的估计,而无需对每种蛋白质进行表达和直接测量。
神经网络的主要缺点是可解释性。神经网络的输出不是描述实际的算法过程,而是对输入算法的数据的解释。它确实有助于我们绘制相关性,这可以为我们提供有关该过程的更多信息。
总之,高通量光散射是筛选和深入表征蛋白质物理稳定性的完美工具。一旦完成,PIPPI数据库将有助于快速评估蛋白质是否适合开发。同样,机器学习算法将提供数据驱动的预测,以通知这些决策,并在新蛋白疗法的开发过程中实现成本节约。
推荐内容
-
全国首例同性伴侣争抚养权案宣判 法院怎么判决
【全国首例同性伴侣争抚养权案宣判 法院怎么判决】我们在生活中听到抚养权案的挺多吧,但是你有听过同性伴侣争抚养权的吗?近日就有一起同
-
百事收购百草味 百草味身价4年翻5倍
百事收购百草味2月23日晚间,好想你(002582)健康食品股份有限公司以7 05亿美元(约合人民币49 53亿元)的价格出售旗下杭州郝姆斯食品有限公司
-
在祈祷螳螂中研究3D视觉
今天发表在Nature Communications上的新研究展示了祈祷螳螂中3D视觉所需神经元的惊人图像。在一个特别设计的昆虫影院中,螳螂配有3D眼镜,
-
这些洗发水的真相你可能并不清楚? 真的是这样吗?
这些洗发水的真相你可能并不清楚? 真的是这样吗?流量为王的时代,信息传播速度越来越快,但其中很多消息还没被证实真实性就大范围传播开
-
放射云、鱼鳞云表示很委屈:预测地震真的与我们无关?真是如此?
随着互联网的快速发展,我们在获取信息的时候很容易被带跑方向。有时候真相也许并不是网上说的那样,所以我们必须要有自己的判断和独立...
-
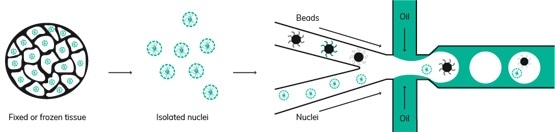
Dolomite Bio为其Nadia仪器引入了高通量sNuc-Seq协议
Dolomite Bio是一家领先的单细胞技术供应商,今天为其Nadia仪器推出了高通量单核RNA测序(sNuc-Seq)方案。Nadia应用产品组合的这一最新成员
-
细数影响睡眠质量的5大谣言? 真实情况是这样
细数影响睡眠质量的5大谣言? 真实情况是这样全民自媒体时代,讯息传播效率飞速提高,但其中很多消息还没被证实真实性就大范围传播开了。