陈薇院士回应疫苗发热率高 陈薇 个人资料简介
随着疫情在全球的爆发,疫苗无疑是我们最重要的武器之一。据最新消息显示,今天就有一则关于陈薇院士回应疫苗发热率高的消息引起了网友们的围观,具体是什么情况呢?下面一起来了解下。
7月28日,陈薇院士在天津市举办的一次活动中,就人腺病毒载体疫苗Ad5-nCo的研制过程,面临的问题作了一个内部报告,首次全方位解读了疫苗研发全过程,并回复了公众对于疫苗副作用高的质疑。这次内部报告发生在康西诺即将上市前夕。


疫苗在3月16日获批,并在当天晚上完成了第一个受试者的接种。 当天全世界只有两个疫苗上临床,一个是我们腺病毒的重组疫苗,一个是美国莫德纳公司(Moderna)mRNA 疫苗。 我们比它早打了五个小时,腺病毒重组疫苗是在北京时间的3月16日,莫德纳公司是在美国时间的3月16日。 (西雅图时间)

武汉一期临床试验共有108人。二期临床试验,四月十二日启动,共有508人接种疫苗。是惟一一个一针见效的疫苗。


3月16日,在武汉、西安、北京三地举行了远程答辨,并获得临床许可。

5月22日,腺病毒重组疫苗一期临床结果在全球领先公布,发表于《柳叶刀》杂志上。

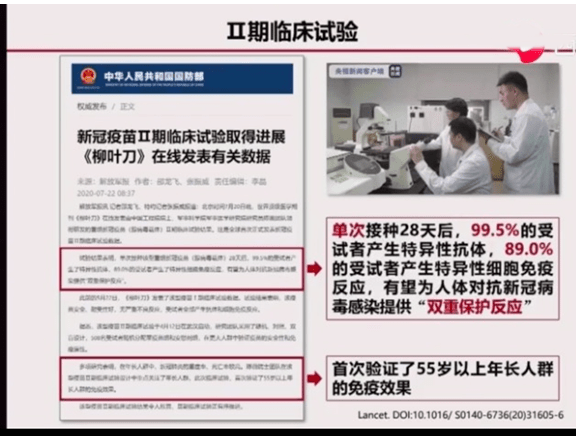
7月20日,冠病疫苗二期(II期)临床试验结果的论文在柳叶刀杂志上刊发,论文显示该疫苗是安全的,并且可以诱发免疫反应。
必须强调的是,前述临床试验的受试者在接种疫苗后,都没有被刻意暴露在感染冠病的危险中,目前尚无法确定该疫苗是否能有效预防冠病感染,而需要进行三期临床试验来回答这一问题。 此外,前述试验仅追踪受试者28天,因此,尚无该疫苗诱导的免疫力持久性数据。
前述二期临床试验的主要目的是,评估疫苗的免疫原性和安全性,并为三期临床试验确定最合适的疫苗剂量提供依据。
前述试验四月份在武汉进行。508名受试者参与其中。13%受试者的年龄在55岁以上。61%受试者的年龄在18岁至44岁之间,26%受试者的年龄在45岁至54岁之间。其中253名受试者接受了高剂量的疫苗,;126人接受了安慰剂,没打疫苗。试验结果显示,接种前述疫苗的高剂量组的95%的受试者,和低剂量组91%的受试者,在接种疫苗后第28天时,均诱发了T细胞免疫反应或抗体免疫反应。
此外,接种后第28天,高剂量组96%的受试者和低剂量组97%的受试者,均出现了结合抗体免疫应答;而中和抗体免疫应答的受试者比例分别是59%和47%。
柳叶刀的论文认为腺病毒重组疫苗,在不良反应方面,注射疫苗后28天内,高剂量组出现三级严重不良反应的受试者一共24人,占比9%;低剂量组一人;安慰剂组两人;其主要症状是发热。大部分受试者出现的不良反应是轻微或中度的,比如发热、疲劳和注射部位疼痛。高剂量组72%的受试者出现了上述症状,低剂量组的比例是74%,安慰剂组的比例是37% 。

目前正在与俄罗斯、巴西、智利和沙特阿拉伯等国就3期试验进行谈判,预期将在8月开展3期试验。
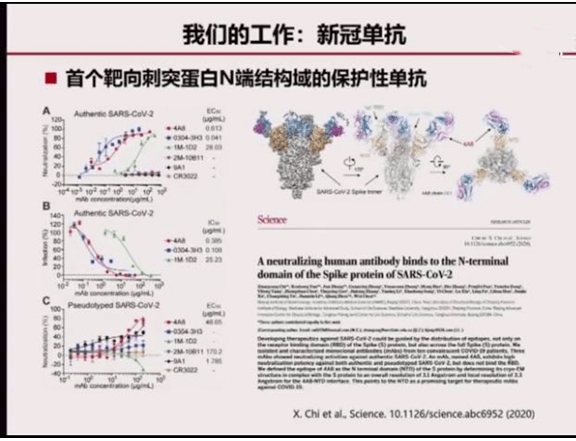
陈院士团队目前正在研究新冠单抗。
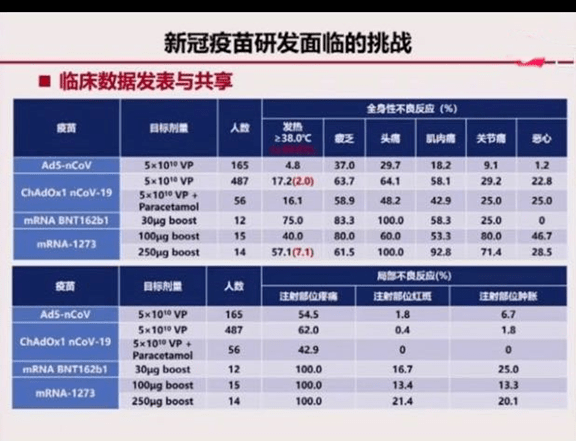

关于腺病毒重组疫苗副作用与安全性的问题,陈薇院士披露,当我们5月22日发表第一份报告时,受到很大的压力,说疫苗副作用大,发热率很高等等。发生这个问题的原因,一是国内外发热标准不一致所致。目前在国外三十八度以上才算发热,但国内三十七度三就算发热,如果以国外三十八度为标准的话,我们目标发热率只有百分之四点八,还有疲乏头痛肌肉痛恶心等,都比其他已发表数据的疫苗低。不管是全身性反应还是局部性反应,都比其他疫苗的数据要弱得多,这些都是以数据来说话。
据了解,陈薇,女,1966年2月26日出生于浙江兰溪,中共党员,生物安全专家,中国工程院院士,中国人民解放军军事科学院军事医学研究院生物工程研究所研究员,专业技术5级,少将军衔。
推荐内容
-
上海4月25日新增本土“1661+15319”,新增本土死亡病例52例
上海4月25日新增本土“1661+15319”,新增本土死亡病例52例 原标题:上海4月25日新增本土“1661+15319”,
-
通过Malaise诱捕样本和DNA条形码监测昆虫生物多样性的效率
1989年至2013年德国专家公民科学家报告的昆虫生物量超过75%的大幅下降证明了迫切需要新的方法和标准进行快速和广泛的生物多样性评估。如果
-
教你川味水煮鱼的做法,麻辣鲜香,开胃下饭,跟饭店的味道有一拼
教你川味水煮鱼的做法,麻辣鲜香,开胃下饭,跟饭店的味道有一拼 原标题:教你川味水煮鱼的做法,麻辣鲜香
-
突破性发展抗病蛋白
X射线和电子显微镜技术有助于展现蛋白质伴侣的故事。X射线晶体学和低温电子显微镜(cryo-EM)的组合有助于协同努力以获得真菌蛋白质Hsp104的
-
创造营2020落下帷幕 虞书欣为张艺凡打call
刚刚 虞书欣为张艺凡打call 的消息登上热搜榜啦!这是怎么回事呢?原来是昨日晚间创造营2020的比赛落下了帷幕,张艺凡以第七名的名次在《创造
-
31省区市新增确诊22例 其中境外输入病例9例
【 31省区市新增确诊27例 : 北京新增确诊22例 】关于31省区市新增确诊22例这个话题,相信小伙伴们是非常有兴趣了解的,因为这个话题是目前
-
产后抑郁症在12个月内会有多严重
一项新的西北医学研究成功地预测了新生母亲在分娩后的第一年内是否会出现恶化的抑郁症状,因为她确定了四种使她处于危险中的母性特征。...
-
10月27日二连浩特额济纳旗疫情最新数据公布 昨日,内蒙古新增本
内蒙古新增本土确诊12例:二连浩特1例、额济纳旗11例。据内蒙古卫健委通报,10月26日8时至10月27日7时,内蒙古自治区报告无新增疑似病例和
-
国家邮政约谈丰巢 国家邮政约谈说了什么?
国家邮政约谈丰巢怎么回事?国家邮政为什么约谈丰巢?近日闹得沸沸扬扬的丰巢收费事件依然在持续发酵,13日,一则关于国家邮政局约谈丰巢负责
-
Phospho-RNA-seq可以获得mRNA和lncRNA片段
根据密歇根大学罗杰尔癌症中心研究人员今天在EMBO杂志上发表的一篇论文,Phospho-RNA-seq是一种新的RNA测序方法,揭示了血浆中数千种以前难