什么阻止了人类细胞中的禽流感
通常,禽流感病毒很难在人与人之间传播。但是,如果确实发生这种情况,则可能引发大流行。MDC和RKI的研究人员现在在《自然通讯》杂志上解释了什么使得从动物到人类的跨越变得不太可能。
每当人们突然感染H5N1,H7N9和H5N6等禽流感病毒时,世界卫生组织(WHO)都必须评估这种风险:这是大流行的最初迹象吗?还是仅通过与受感染的家禽密切接触才出现几十或几百例病例?麦克斯·德尔布吕克分子医学中心(MDC)的马蒂亚斯·塞尔巴赫(Matthias Selbach)教授领导的研究人员现在发现了另一个谜题,这一谜题在这一初步评估中可能很重要。在《自然通讯》上发表的一篇论文中,研究人员解释说禽流感A病毒(IAV)无法将受感染的人类细胞转化为有效的病毒。因为它们在感染后不能产生足够的基质蛋白M1。但是,该病毒需要这种蛋白质才能从细胞核中导出其遗传物质的许多副本,这是构建新病毒的前提。
并非所有流感都是一样的-名称指的是一大类病毒。该家族的每个成员都以在病毒表面上的两个刺状生长而命名:血凝素(H)使神经病毒能够感染可繁殖的人和动物细胞,神经氨酸酶(N)则有助于病毒的后代自我提取来自被感染细胞。在水禽中,有16种已知的血凝素亚型和9种已知的神经氨酸酶亚型。这样就产生了至少144种可能的组合,这些组合不断变化并适应新的宿主,例如鸡,但也包括哺乳动物,包括马,猪和人。
这种新的病毒变种通常比季节性流感更具危险性,因为人类免疫系统以前从未遇到过它们。有些人发现自己无法防御,而其他人的免疫系统反应如此剧烈,以至于人自身的抵抗力会损害身体。在最坏的情况下,大流行可能会使数百万人丧生。例如,1918年的西班牙流感造成了5000万以上的受害者。因此,全世界的研究人员都在试图了解确定何时可能发生大流行,何时不可能发生大流行的规则。
为什么人类细胞对禽流感有害的病毒工厂?
塞尔巴赫解释说:“例如,人类和鸟类中的血凝素化学结构略有不同,这使得禽流感病毒比人的细胞更难以渗透人细胞。” Boris Bogdanow,博士 塞尔巴赫研究小组的学生,也是本研究的主要作者,他的研究专门针对流感病毒中存在的其他自然物种屏障。
Matthias Selbach的小组使用定量质谱分析蛋白质。Boris Bogdanow和他的同事与罗伯特·科赫研究所(RKI)合作,分别用禽流感病毒和人流感病毒感染了人肺上皮细胞。然后,他们在质谱仪中测量了所有新产生的蛋白质的量。博士后研究员Katrin Eichelbaum博士还开发了一种能够精确区分新旧蛋白质的方法。Boris Bogdanow报告说:“在第一个分析中,我们没有发现这两种菌株之间有任何重大差异。“乍看之下,禽流感病毒和人类病毒在蛋白质生产方面几乎没有差异,这非常令人惊讶。”
但是细节在于魔鬼,因此Bogdanow进行了更深入的分析,以更仔细地观察蛋白质的分布。为此,他遇到了基质蛋白M1,该基质蛋白M1在感染人病毒的肺细胞中产生的数量更多。M1蛋白尤其负责从受感染细胞的核中输出复制的病毒RNA,然后将其与其他新产生的病毒蛋白组装在一起,形成流感病毒的后代。那么,是因为存在的M1蛋白太少,人类细胞中禽流感病毒的病毒RNA是否仍被困在细胞核中?
另一个难题
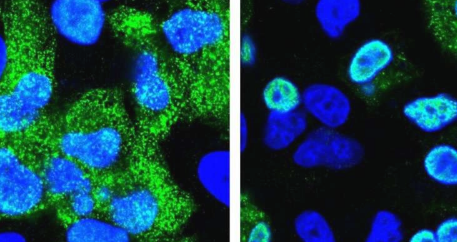
荧光显微镜研究证实了这些怀疑。禽流感病毒的遗传物质远没有人类流感病毒的RNA分裂出细胞核的能力。但为什么?在MDC的测序平台和Irmtraud Meyer教授的帮助下,他们在禽流感病毒的病毒RNA中发现了一个小片段,该片段影响了选择性剪接。Bogdanow说:“我们称其为顺式调节成分。” “选择性剪接可调节最终由单个基因产生的蛋白质,因为许多基因编码的蛋白质不止一种。当人类细胞受到禽流感的攻击时,该元素可确保产生更多的M2而不是M1 蛋白。”
为了评估此结果的相关性,罗伯特·科赫研究所的Thorsten Wolff教授及其研究小组将顺式调控元件从禽流感病毒转移到了人类病毒。确实确实导致了人类流感病毒在人肺细胞中复制的效率降低。塞尔巴赫的团队甚至对西班牙流感病毒进行了类似的实验,该病毒的遗传物质于九十年代从阿拉斯加永久冻土的坟墓中分离出来。但是,他们只使用了病毒RNA的一小部分,而不是整个病毒。然而,他们也能够证实其关于这种病毒的顺式调控元件的理论。
塞尔巴赫说:“禽流感病毒的致病性及其是否具有大流行潜力,当然取决于许多因素。” “关于细胞培养的研究不能涵盖所有这些因素。但是,将来在禽流感病毒的风险评估中包括对该RNA片段的分析可能会很有用。”
推荐内容
-
为什么大街小巷的药店越来越多?药店是靠啥来赚钱?告诉你真相
为什么大街小巷的药店越来越多?药店是靠啥来赚钱?告诉你真相 现在去药店买药,常常会遇到这样的情况:只是单纯地想买个感冒药,但是
-
基因工程的应用有哪些 等待你的进一步研究
伴随着基同技术日益发达,已经得到了一定的应用,具体有哪些?这个应用真的行之有效吗?让我们一起去看看都有哪些吧!植物基因工程可以让植物
-
封控在家太久,焦虑暴躁怎么办?专家给出6点建议
封控在家太久,焦虑暴躁怎么办?专家给出6点建议 今天上午10:00上海市举行第178场新冠肺炎疫情防控新闻发布会▽上海封控时间比较长,
-
推动DNA测序的界限
在新墨西哥大学(UNM)创建的一家开发技术的年轻公司正致力于破坏DNA测序领域。Armonica Technologies,LLC正在开发一种DNA测序平台,可在几
-
“现挤奶”既不营养也不安全,别喝!?你知道哪些
日常生活中我们经常会听到各种各样的坊间流言。然而很少人去求证这些流言的真实性,久而久之就变成了真事。在这里,小编必须提醒大家,...
-
经常吃菠菜豆腐汤容易引起肾结石??听听专家怎么说
生活中我们经常会听见各种各样的流言,但是只要我们用心去思考和辨认其实 不难发现这些谣言有很多破绽。所以今天,小编照常给大家辟谣一则
-
双相情感障碍小鼠模型中昼夜节律基因的红外振荡
情绪和情绪相关行为变化的分子基础尚不清楚。日本的研究人员通过研究双相障碍小鼠模型中大脑中的基因表达模式,成功地预测了类似情绪变...
-
贵阳九价HPV疫苗开启摇号
贵阳九价HPV疫苗开启摇号 贵阳市的小姐姐们你们等待已久的九价HPV疫苗终!于!来!了!一次摇中,就可以打完3针为了提高贵阳市九价HPV疫苗
-
iclaprim治疗急性细菌性皮肤及皮肤结构感染遭FDA拒绝
Motif Bio是一家专注于新型抗生素研发的临床阶段生物制药公司。近日,该公司宣布已收到美国食品和药物管理局(FDA)关于iclaprim治疗急性细